You have no items in your shopping cart.
解码ABC转运蛋白——跨膜运输的超级家族
从细菌到人类,所有生物体内都活跃着一类关键的膜蛋白——ABC转运蛋白。作为最大的跨膜蛋白超家族之一,它们通过保守的ATP结合盒(ATP-binding cassette) 结构域水解ATP获取能量,驱动底物跨越细胞膜。
🔬 多功能运输系统
ABC转运蛋白可转运多种物质:
✅ 营养物质与代谢产物
✅ 肽类、脂质、多糖
✅ 药物及外源毒素(⚠️ 肿瘤多重耐药的核心机制)
这类蛋白参与营养吸收、渗透调节、免疫应答等关键生理过程。其功能异常直接导致多种遗传病。
典型案例:囊性纤维化患者因 CFTR蛋白(ABCC7亚型) 基因突变,导致氯离子转运障碍,引发肺部黏液积聚及呼吸衰竭。
🧬 ABC转运蛋白亚家族分类图谱
人类基因组编码 49个ABC转运蛋白,根据结构进化分为七类:
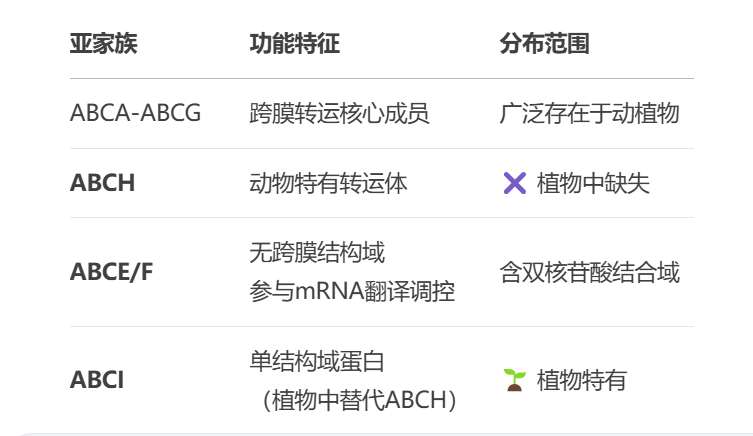
ABC转运蛋白的结构特征
ABC转运蛋白的经典结构包括:
两个核苷酸结合域(NBD):高度保守,负责结合和水解ATP,为转运提供能量。
两个跨膜结构域(TMD):形成跨膜通道,负责底物识别与运输。
ABC转运蛋白三类结构构型:
1.全分子转运体
是单条多肽链,包含:
▫️ 两个核苷酸结合域(NBD)
▫️ 两个跨膜结构域(TMD)
典型排列:TMD1-NBD1-TMD2-NBD2(正向)或 NBD1-TMD1-NBD2-TMD2(反向)
2.半分子转运体
是单条多肽链,含:
▫️ 一个NBD + 一个TMD
通过同源/异源二聚化形成功能单元
3.可溶性蛋白
NBD与TMD位于不同肽链(ABCE/F亚型)
专司翻译调控等非转运功能
ABC转运蛋白转运方向
ABC转运蛋白的转运方向大致分为两类:
将底物从细胞内运出:广泛存在于真核和原核生物中。
将底物运进细胞内:主要存在于原核生物中,通常需要额外的底物结合蛋白(SBP)将底物递送至TMD。
在革兰氏阴性菌中,SBP位于周质间隙。
在革兰氏阳性菌和古细菌中,SBP与膜相关或与转运蛋白复合物融合。
ABC转运蛋白物种分布和数量
迄今为止, 已在人类 (Homo sapiens)基因组中发现49个ABC转运蛋白, 酵母(Saccharomyces cerevisiae)中大约有30个ABC转运蛋白, 大肠杆菌中已发现79个ABC转运蛋白成员。与其他生物相比, 植物ABC 转运蛋白数目相对较多, 以水稻(Oryza sativa)和拟南芥(Arabidopsis thaliana)为代表的ABC转运蛋白家族成员多达130种以上, 这可能是植物在长期进化过程中适应复杂环境的结果。
人类健康与医学价值
癌症中的“多药耐药性”主要由各种机制驱动,包括 ATP 结合盒 (ABC) 转运蛋白(如 P-糖蛋白 (ABCB1))的过表达,这些转运蛋白主动将化疗药物从癌细胞中泵出,从而降低其细胞内浓度和有效性。此外,一些其他的因素也导致了多药耐药性的发生。
多药耐药性的复杂性不仅使治疗方案复杂化,而且还导致癌症的高死亡率。了解多药耐药性的潜在机制并制定克服这种耐药性的策略对于改善患者预后至关重要。
人类 ABC 转运蛋白 ABCB1 (hP-gp) 赋予多药耐药性的标志是多种药物的识别和外排,但多特异性的确切机制仍未解决。
🔬 Biorbyt提供科研级、高纯度的ABC蛋白的多种亚型产品,供科研人员解析这些蛋白的结构与功能机制,为攻克癌症、遗传病及耐药性问题提供新路径。
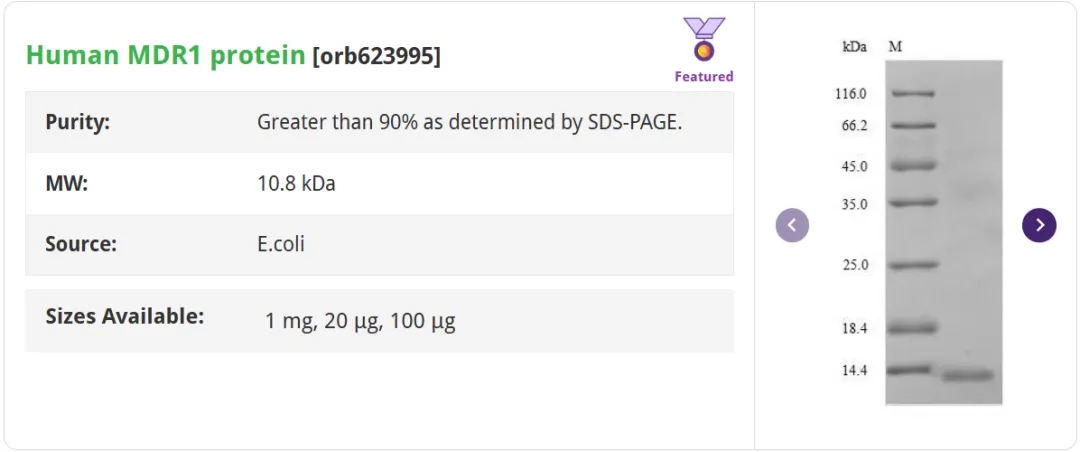
Human MDR1 protein,ABCB1[ orb623995]
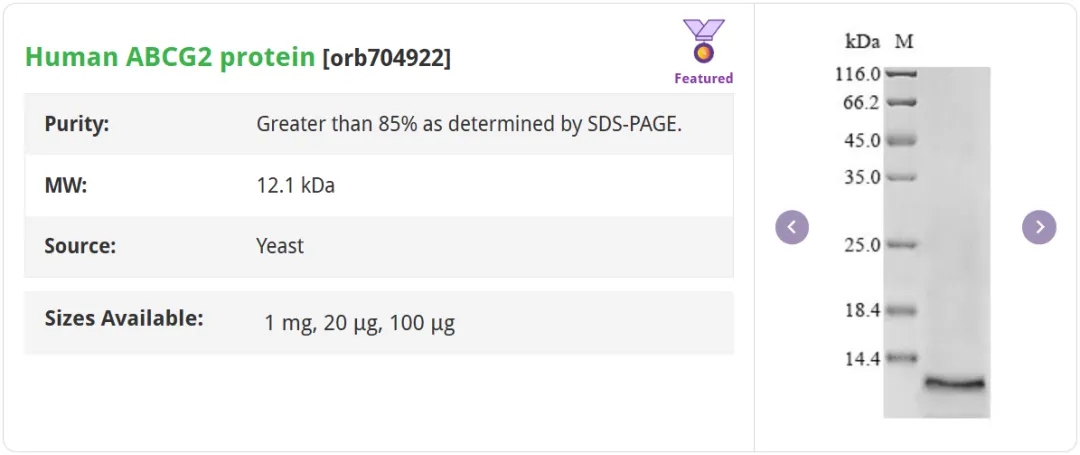
Human ABCG2 protein [orb704922]
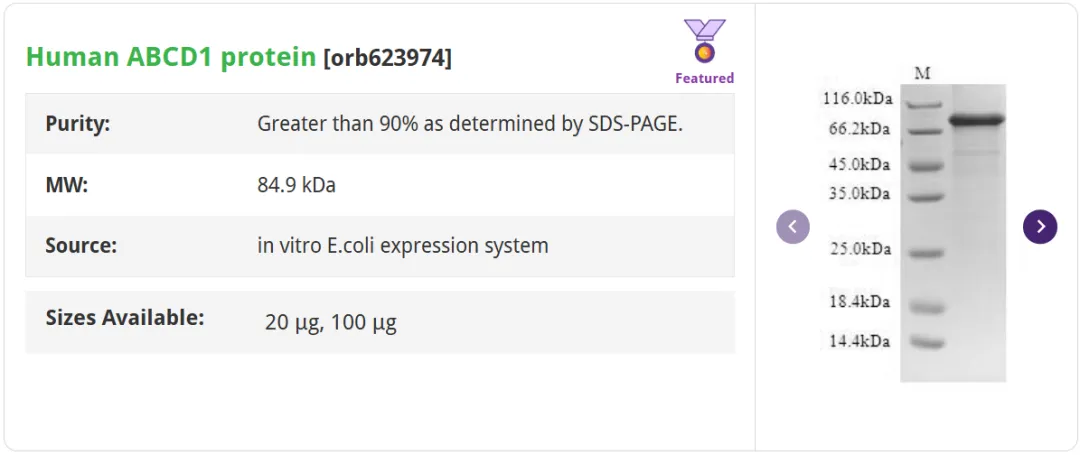
Human ABCD1 protein [orb623974]
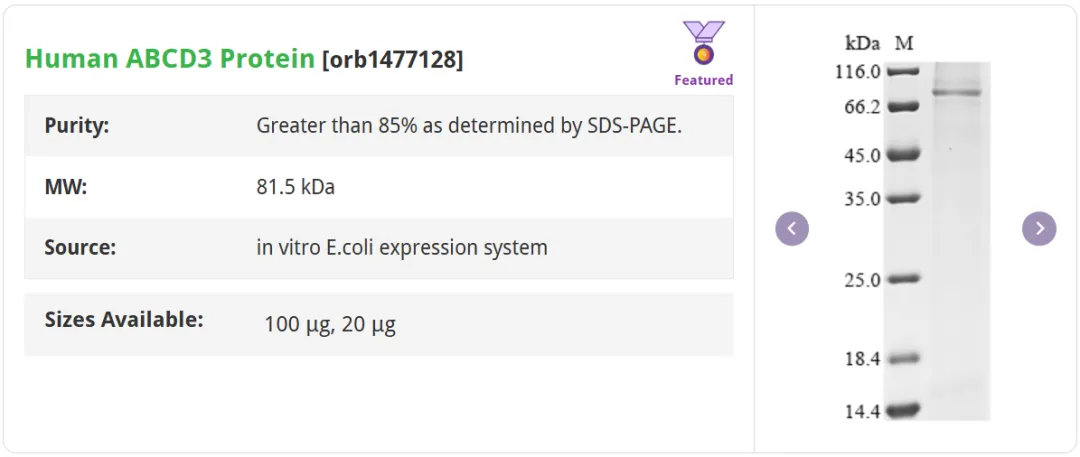
Human ABCC1 protein [orb419225]
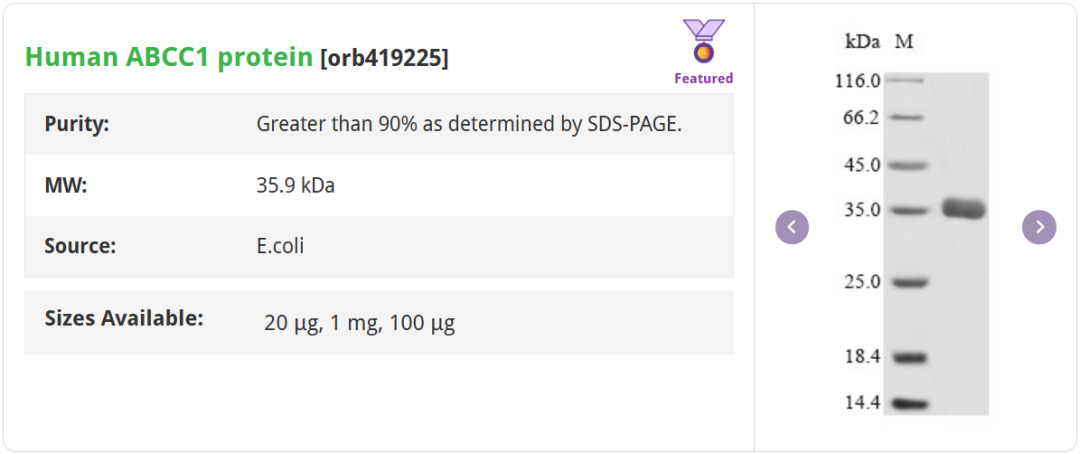
Human ABCG1 protein [orb605290]
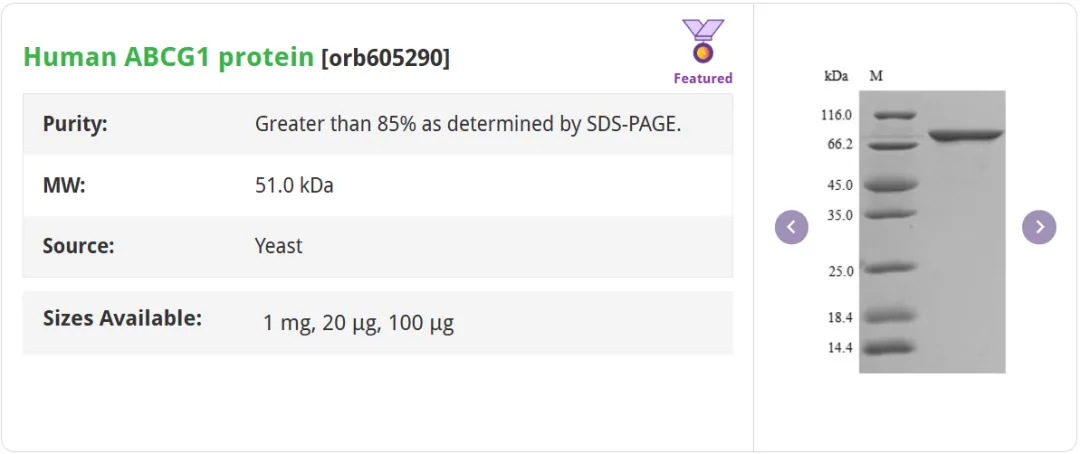
Human ABCB8 protein [orb54691]
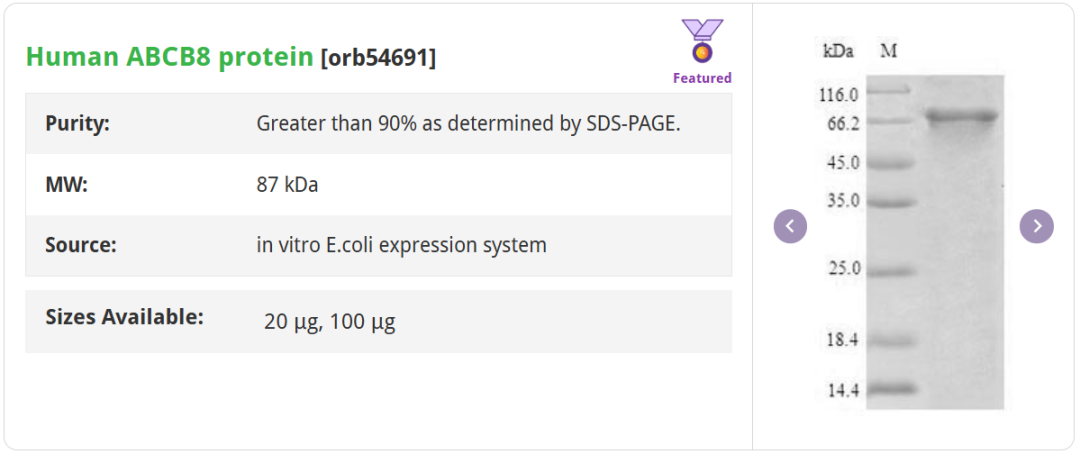
Human ABCD3 Protein [orb1477128]
更多产品,欢迎咨询我们!
参考文献:
1.https://www.mdpi.com/1422-0067/26/13/6119
2.https://www.sciencedirect.com/science/article/pii/S0022283625001482?via%3Dihub
2.王晓珠,孙万梅,马义峰,韩二琴,韩丽,孙丽萍,彭再慧,王邦俊.拟南芥ABC转运蛋白研究进展[J].植物生理学报,2017,53(2):133-144
